المقدمة
في عصر الطب الشخصي، لم يعد التعامل مع مرض السرطان يعتمد على التشخيص السريري وحده. لقد أحدثت التطورات في علوم الجينوم والوراثة ثورة حقيقية، حيث أصبح فحص البصمة الجينية أو ما يُعرف بـ **الفحص الجيني للسرطان** من أهم وأحدث الأساليب الطبية في عالم تشخيص وعلاج الأورام. يعتمد هذا الفحص على تحليل الحمض النووي (DNA) بدقة متناهية بهدف اكتشاف الطفرات الجينية المسؤولة عن تطور السرطان أو التي تزيد من خطورة الإصابة به، مما يفتح الباب أمام استراتيجيات علاجية أكثر فاعلية وتخصيصًا.
تكمن أهمية هذا الفحص اليوم في دوره الكبير في توجيه التشخيص الدقيق، وتحديد العلاج الأنسب لكل مريض بشكل فردي، وتوقع استجابة الورم للعلاج، وهو ما جعل استخدامه جزءًا أساسيًا من البروتوكولات العالمية في طب الأورام الحديثة. هذا المقال هو دليلك الشامل لفهم ماهية الفحص الجيني، تقنياته المتقدمة، الفرق بين أنواعه، ودوره المحوري في تحسين نتائج علاج مرضى السرطان.

ما هو فحص البصمة الجينية (التحليل الجيني للأورام)؟
فحص البصمة الجينية، أو **التحليل الجيني للأورام**، هو تحليل مُتقدّم يهدف إلى دراسة التغييرات الجينية (Genetic Mutations) الموجودة داخل الخلايا السرطانية أو في الخلايا السليمة للجسم. هذه التغييرات هي التي توجه نمو الورم وانتشاره وتحدد نقاط ضعفه. يمكن تصنيف هذه الطفرات الجينية إلى نوعين رئيسيين:
الطفرات الوراثية (Inherited Mutations):
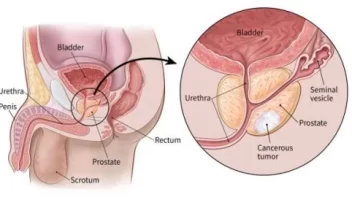
هي الطفرات التي تنتقل من أحد الوالدين وتكون موجودة في كل خلية من خلايا الجسم. هذه الطفرات لا تعني بالضرورة الإصابة بالسرطان، لكنها تزيد من **خطورة الإصابة بالسرطان** بشكل كبير. أشهر الأمثلة عليها هي طفرات جينات *BRCA1* و *BRCA2*، المرتبطة بشكل وثيق بزيادة احتمالية الإصابة بسرطان الثدي، وسرطان المبيض، وسرطان البروستات، وسرطان البنكرياس.
الطفرات المكتسبة (Somatic Mutations):
هي الطفرات التي تحدث في الحمض النووي لخلية واحدة أو مجموعة من الخلايا خلال حياة الشخص نتيجة التعرض لمجموعة من العوامل البيئية أو الداخلية. تشمل هذه العوامل التعرض للتدخين، المواد الكيميائية، الأشعة فوق البنفسجية، أو أخطاء تحدث أثناء انقسام الخلية. هذه الطفرات هي التي تُسبب تطور الورم وهي الهدف الأساسي لـ **العلاج الموجه للسرطان**.
يهدف الفحص الجيني إلى تحديد هذه الطفرات، سواء كانت وراثية أم مكتسبة، لتوفير خريطة دقيقة للورم.
الأهداف الرئيسية لـ فحص الجينات للسرطان
يتجاوز الهدف من الفحص الجيني مجرد التشخيص التقليدي، حيث يقدم رؤى حاسمة تؤثر على مسار العلاج بالكامل. تشمل الأهداف الرئيسية لـ **فحص الجينات للسرطان** ما يلي:
1. توجيه خطة العلاج (Targeting Therapy):
- **اختيار العلاج الموجه (Targeted therapy):** يحدد الفحص الطفرات الجينية التي يمكن استهدافها بأدوية محددة تعمل على إيقاف نمو الخلايا السرطانية دون الإضرار بالخلايا السليمة. على سبيل المثال، الكشف عن طفرة *EGFR* في سرطان الرئة يوجه الطبيب لاستخدام مثبطات *EGFR*.
- **تحديد الاستجابة للعلاج المناعي:** بعض الطفرات أو مؤشرات عدم الاستقرار الجيني (مثل TMB و MSI) تحدد ما إذا كان المريض سيستفيد من العلاج المناعي (Immunotherapy) أم لا.
2. التنبؤ بسلوك الورم (Prognosis):
- **التنبؤ بالمسار المستقبلي للمرض:** يساعد الفحص في توقع سلوك الورم، هل سيكون عدوانيًا سريع الانتشار أم بطيء النمو.
- **توقع استجابة المريض للأدوية:** يساعد في معرفة احتمالية استجابة المريض للعلاج الكيميائي أو الإشعاعي، مما يقلل من العلاجات غير الضرورية والآثار الجانبية المصاحبة.
3. الكشف عن السرطان الوراثي (Hereditary Cancer Risk):
- **التمييز بين السرطان الوراثي وغير الوراثي:** يساعد الفحص في تحديد ما إذا كانت الإصابة ناتجة عن طفرة وراثية يمكن أن تنتقل لأفراد الأسرة.
- **إدارة المخاطر:** يتيح للأقارب المعرضين للخطر اتخاذ إجراءات وقائية، مثل الفحص المبكر المتكرر أو الجراحة الوقائية.
المراحل التفصيلية لإجراء فحص البصمة الجينية
تعتبر عملية إجراء **فحص البصمة الجينية** عملية معقدة ودقيقة تتم في مختبرات متخصصة. على الرغم من اختلاف طريقة جمع العينة، إلا أن العملية المخبرية تمر بمراحل قياسية:
1. جمع العينة ونوعيتها: العينة هي أساس الدقة
تُجمع العينة عادةً بطريقتين رئيسيتين:
- **عينة نسيج (Biopsy):** هي الطريقة الأكثر شيوعاً وتفضيلاً للدقة الأولية. تُسحب عينة صغيرة من الورم مباشرة، وتُستخدم هذه العينة للتحليل الجيني المباشر للخلايا السرطانية.
- **عينة دم (Liquid Biopsy):** تُستخدم في تحليل الحمض النووي الحر المتداول في الدم (cfDNA) أو الحمض النووي للأورام المتداول (ctDNA).
2. استخلاص الحمض النووي (DNA Extraction):
تعتبر هذه المرحلة حاسمة لضمان جودة التحليل. يتم فصل الحمض النووي من الخلايا أو من البلازما (في حالة فحص الدم) باستخدام تقنيات ومواد كيميائية مخبرية دقيقة تهدف إلى الحصول على كمية كافية ونقية من الـ DNA.
3. التحليل الجيني واستخدام تقنيات NGS المتقدمة
تعتمد دقة الفحص الجيني على التكنولوجيا المستخدمة في قراءة التسلسل الجيني. هنا يبرز دور التقنيات الحديثة:
تقنية تسلسل الجيل التالي (NGS – Next Generation Sequencing)
تعتبر تقنية NGS هي المعيار الذهبي للتحليل الجيني الشامل. تسمح هذه التقنية المتقدمة بـ:**
- **الكشف الشامل:** الكشف عن مئات الجينات دفعة واحدة في تحليل واحد (Gene Panels).
- **السرعة والدقة:** قراءة تسلسل الحمض النووي بسرعة عالية وبتكلفة أقل مما كانت عليه في السابق.
- **اكتشاف طفرات نادرة:** قدرتها على اكتشاف الطفرات الجينية النادرة أو الجديدة التي قد لا تُكشف بالتقنيات القديمة.
تقنية تفاعل البوليميراز المتسلسل (PCR)
تُستخدم للكشف عن طفرات محددة ومعروفة مسبقًا، مثل طفرة واحدة أو اثنتين. وهي سريعة ومناسبة للحالات التي تتطلب نتيجة سريعة أو عندما يكون الهدف هو البحث عن طفرة متوقعة.
4. قراءة النتائج وتفسير التقرير النهائي
بعد اكتمال عملية التسلسل، يتم تحليل البيانات الجينية الهائلة باستخدام برامج حاسوبية متخصصة (Bioinformatics).
- **المقارنة بقواعد البيانات:** يتم مقارنة النمط الجيني للمريض ببيانات عالمية ضخمة (مثل بيانات COSMIC و ClinVar) لمعرفة تأثير الطفرة المكتشفة على وظيفة البروتين وعلاقتها بالمرض.
- **تفسير التقرير النهائي:** هذه الخطوة يقوم بها طبيب الأورام أو مختص الوراثة. يتم ربط الطفرات المكتشفة بـ **التشخيص الدقيق**، و**خطة العلاج الموجه**، و**التوقعات المستقبلية للمرض (Prognosis)**.

الفرق الجوهري بين فحص الجينات عبر الدم (Liquid Biopsy) وفحص الأنسجة
يعد التمييز بين فحص الدم وفحص الأنسجة أحد الجوانب الهامة التي يجب فهمها عند إجراء **التحليل الجيني للأورام**. لكل منهما دوره ومميزاته.
أولًا: فحص الدم (Liquid Biopsy) – التحليل غير الجراحي
يعتمد **فحص جينات الدم** على تحليل الحمض النووي للخلايا السرطانية المنتشرة في مجرى الدم (ctDNA)، والتي تطلقها الخلايا السرطانية الميتة أو المتحللة.
- **المميزات الأساسية:**
- **سهل وسريع وغير مؤلم:** لا يتطلب أي إجراء جراحي أو تخدير، وهو مثالي للمرضى الضعفاء أو الذين يعانون من أمراض أخرى.
- **متابعة تطور المرض (Monitoring):** مفيد جدًا لمتابعة تطور المرض والاستجابة للعلاج، حيث يمكن إجراؤه بشكل متكرر للكشف عن ظهور طفرات مقاومة جديدة.
- **تجنب الخزعة الصعبة:** مثالي للمرضى الذين يصعب أخذ خزعة منهم، خاصة في حالة أورام العظام أو الدماغ.
- **الكشف عن تغاير الورم (Tumor Heterogeneity):** يظهر تغيرات الورم مع الوقت وفي أماكن انتشاره المختلفة.
- **القيود (العيوب):**
- قد لا يكشف كل الطفرات، خصوصًا إذا كانت كمية الـ DNA السرطاني قليلة جدًا، كما في السرطانات المبكرة.
- أقل دقة في تحديد خصائص الورم في المراحل المبكرة جدًا مقارنة بفحص الأنسجة.
ثانيًا: فحص الأنسجة (Tissue Biopsy) – المعيار الذهبي
يعتمد **فحص الأنسجة** على فحص الخلايا السرطانية مباشرة من الورم الأساسي أو النقائل (Metastases).
- **المميزات الأساسية:**
- **أدق فحص جيني على الإطلاق:** يوفر أكبر كمية من الحمض النووي للورم، مما يضمن أعلى دقة.
- **يكشف خصائص الورم بالكامل:** مناسب للتحليل الجيني الشامل (Comprehensive gene panels) وكشف المؤشرات المعقدة مثل طفرات الأندماج (Fusions) التي يصعب كشفها بالدم.
- **التشخيص الأولي:** هو الطريقة المفضلة عند التشخيص الأولي للمرض.
- **القيود (العيوب):**
- يتطلب إجراء جراحي صغير (خزعة)، مما قد يسبب ألماً أو مضاعفات بسيطة.
- قد لا تكون العينة كافية للتحليل الكامل في بعض الأحيان (Insufficient Tumor Content).
- لا يمكن تكراره بسهولة لمتابعة الاستجابة للعلاج.
متى يُنصح بإجراء فحص البصمة الجينية؟
أصبح الفحص الجيني ضرورة طبية في كثير من الحالات، ولا يقتصر فقط على مرضى السرطان المتقدم. يُوصى بإجراء الفحص في الحالات التالية:
1. حالات الاشتباه بالسرطان الوراثي:
- **وجود تاريخ عائلي قوي للإصابة بالسرطان:** خاصة إذا كان المرض قد ظهر في عدة أجيال أو لدى العديد من أفراد الأسرة.
- **ظهور المرض في عمر صغير:** خاصة قبل سن الخمسين.
- **الإصابة بسرطانات نادرة** أو متعددة الأنسجة.
2. التخطيط العلاجي للسرطانات الشائعة:
يعد الفحص الجيني ضروريًا قبل البدء بأي علاج موجه، خاصة في أنواع السرطان التي أثبتت الدراسات ارتباطها المباشر بطفرات قابلة للاستهداف:
- **سرطان الرئة (Lung Cancer):** للكشف عن طفرات *EGFR*، *ALK*، *ROS1* وغيرها.
- **سرطان القولون والمستقيم (Colorectal Cancer):** للبحث عن طفرات *KRAS*، *NRAS*، و *BRAF*.
- **سرطان الثدي (Breast Cancer):** للبحث عن *HER2* وطفرات *BRCA* الوراثية والمكتسبة.
- **سرطان الجلد (Melanoma):** للبحث عن طفرة *BRAF*.
3. حالات المقاومة العلاجية:
- **عند عدم استجابة المريض للعلاج التقليدي:** إذا فشل العلاج الكيميائي أو الإشعاعي التقليدي، قد يوجه الفحص الجيني لاستخدام خط علاجي جديد موجه.
- **في حالة الانتكاس (Recurrence):** لإعادة تقييم الطفرات، فقد تكون الخلايا السرطانية قد طورت طفرة مقاومة جديدة.
دقة وموثوقية فحص البصمة الجينية (هل النتائج دقيقة؟)
تعتبر دقة **الفحص الجيني للسرطان** واحدة من أعلى مستويات الدقة في التشخيص الطبي الحديث. يعتمد عليها الأطباء عالميًا لأنها تقدم بيانات كمية ونوعية حول التغيرات الجينية بدلاً من الاعتماد على الخصائص المظهرية للخلايا.
تقنية NGS وضمان الموثوقية:
عند استخدام تقنية **NGS** الحديثة، وخاصة على عينة نسيجية عالية الجودة، تصل دقة الكشف عن الطفرات إلى مستويات ممتازة. أما فحص الدم، فقد تحسنت دقته بشكل كبير وأصبح يُستخدم بثقة لمتابعة المرض واكتشاف الانتكاسات المبكرة.
تأثير الدقة على القرار العلاجي:
تشير الدراسات واسعة النطاق إلى أن الفحص الجيني يوجه ما يتراوح بين **70% و 80% من القرارات العلاجية** في الأورام الحديثة. هذا يعني أن القرار بتغيير نوع العلاج، أو إضافة علاج موجه، أو الدخول في تجربة سريرية يعتمد بشكل مباشر على نتائج هذا الفحص.
في كثير من الحالات، يكون الفحص الجيني سببًا مباشرًا في **تحسّن نتائج العلاج وزيادة نسب الشفاء**، لأنه يضمن أن المريض يحصل على العلاج الذي صُمم خصيصًا للطفرات الموجودة في ورَمه.
نقاط القوة الأساسية والدور المستقبلي للتحليل الجيني
يُمثل **التحليل الجيني للأورام** القوة الدافعة للطب الشخصي (Precision Medicine)، وتتجلى نقاط قوته فيما يلي:
1. تمكين العلاج الدقيق الموجّه (Targeted Therapy):
- يساعد في اختيار علاج دقيق موجّه للطفرة الجينية المحددة، مما يزيد من فعالية العلاج ويقلل الآثار الجانبية الشديدة.
- يقلل من العلاج غير الضروري الذي لن يستفيد منه المريض، موفراً الوقت والجهد والموارد.
2. المراقبة الشاملة للمرض (Comprehensive Monitoring):
- يساعد في مراقبة المرض وتحديد احتمال عودته بعد العلاج بوقت طويل، خاصة عند استخدام فحص الدم الدوري (Liquid Biopsy).
- يكشف عن السرطانات الوراثية المبكرة، مما يسمح بالتدخل الوقائي.
3. الدخول في التجارب السريرية (Clinical Trials):
تعتمد العديد من الأدوية الجديدة الواعدة في التجارب السريرية على استهداف طفرات جينية محددة. نتائج الفحص الجيني هي المفتاح لتأهيل المريض للدخول في هذه التجارب، مما يتيح له الوصول إلى أحدث العلاجات قبل توفرها التجاري.
4. التشخيص الدقيق (Accurate Diagnosis):
يعطي تشخيصًا أدق لنوع الورم وتصنيفه البيولوجي الجزيئي، وهو التصنيف الذي أصبح أكثر أهمية من التصنيف النسيجي التقليدي في كثير من الأحيان.
تحديات التحليل الجيني والتفسير السريري
على الرغم من التطور الهائل، يواجه تطبيق الفحص الجيني بعض التحديات التي يعمل العلماء والأطباء على تجاوزها:
1. التغايرية الورمية (Tumor Heterogeneity):
ليست كل الخلايا في الورم متطابقة جينيًا. الخزعة المأخوذة من جزء واحد قد لا تمثل الصورة الجينية الكاملة للورم أو نقائله. هذا هو أحد الأسباب التي دفعت إلى تطوير فحص الدم (Liquid Biopsy) لمواجهة هذه التغايرية.
2. الطفرات ذات الأهمية غير المعروفة (VUS):
في بعض الأحيان، يكتشف الفحص طفرات لم يتم تحديد دورها السريري أو المرضي بشكل كامل بعد (Variants of Uncertain Significance). يتطلب تفسير هذه الطفرات مجهودًا كبيراً ومتابعة لقواعد بيانات عالمية حديثة.
3. التكلفة والتغطية التأمينية:
قد تكون تكلفة التحليل الجيني الشامل (NGS) مرتفعة، ولا تغطيها جميع أنظمة التأمين الصحي بالكامل، على الرغم من أن تكلفة العلاج غير الفعال تفوق تكلفة الفحص الجيني في كثير من الأحيان.
الخلاصة والآفاق المستقبلية لـ فحص البصمة الجينية
يُعد **فحص البصمة الجينية** خطوة أساسية لا غنى عنها في عالم تشخيص السرطان ووضع خطة علاج مناسبة في العقد الحالي. لقد انتقلنا من نموذج “علاج واحد يناسب الجميع” إلى نموذج **الطب الشخصي الدقيق**، حيث يكون القرار العلاجي مدفوعًا بخريطة جينية فريدة لكل مريض.
هذا الفحص المتقدم لا يساعد فقط على **فهم طبيعة الورم بشكل دقيق** واختيار العلاج الأنسب والأكثر فعالية، بل يساهم بشكل مباشر في **تحسين فرص الشفاء** وتقليل العبء الناتج عن العلاج غير الضروري. ومع استمرار تطور تقنيات الجيل التالي (NGS) وظهور أجيال جديدة من الأدوية الموجهة، فإن الدور المحوري لـ **التحليل الجيني للأورام** سيستمر في النمو، ليصبح الأمل الأكبر للمرضى والأطباء في معركتهم ضد السرطان.
إذا كنت أنت أو أحد أفراد عائلتك تواجه تشخيص السرطان، فإن استشارة طبيب الأورام حول إجراء الفحص الجيني الشامل هي الخطوة الأولى والأهم لضمان الحصول على **أفضل وأدق خيارات العلاج الموجه** المتاحة عالميًا.