la introducción
En la era de la medicina personalizada, abordar las enfermedades ya no es... cáncer Se basa exclusivamente en el diagnóstico clínico. Los avances en genómica y genética han revolucionado este campo, convirtiendo la huella genética, o prueba genética del cáncer, en una de las técnicas médicas más importantes y avanzadas para el diagnóstico y tratamiento de tumores. Esta prueba se basa en un análisis de ADN de alta precisión para detectar mutaciones genéticas responsables del desarrollo del cáncer o que aumentan el riesgo de desarrollarlo, abriendo así la puerta a estrategias de tratamiento más eficaces y personalizadas.
La importancia de esta prueba hoy en día reside en su papel crucial para guiar un diagnóstico preciso, determinar el tratamiento más adecuado para cada paciente y predecir la respuesta del tumor al tratamiento. Esto ha convertido su uso en una parte esencial de los protocolos globales en oncología moderna. Este artículo es una guía completa para comprender qué son las pruebas genéticas, sus técnicas avanzadas, las diferencias entre sus tipos y su papel fundamental para mejorar los resultados de los pacientes con cáncer.

¿Qué es la huella genética (análisis genético de tumores)?
La huella genética, o **análisis genético tumoral**, es un análisis avanzado que busca estudiar las mutaciones genéticas presentes en las células cancerosas o en las células sanas del organismo. Estas mutaciones guían el crecimiento y la propagación del tumor e identifican sus vulnerabilidades. Estas mutaciones genéticas se pueden clasificar en dos tipos principales:
Mutaciones hereditarias:
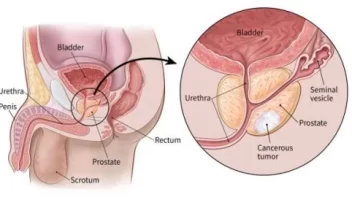
Estas son mutaciones que se transmiten de padres a hijos y se encuentran en cada célula del cuerpo. Estas mutaciones no implican necesariamente el desarrollo de cáncer, pero sí aumentan significativamente el riesgo de desarrollarlo. Los ejemplos más comunes son las mutaciones en los genes BRCA1 y BRCA2, que están estrechamente relacionadas con un mayor riesgo de cáncer de mama, ovario, próstata y páncreas.
Mutaciones somáticas:
Se trata de mutaciones que se producen en el ADN de una sola célula o de un grupo de células a lo largo de la vida de una persona como resultado de la exposición a diversos factores ambientales o internos. Estos factores incluyen la exposición al tabaco, a sustancias químicas, a la radiación ultravioleta o a errores que ocurren durante la división celular. Estas mutaciones son las que causan el desarrollo de tumores y constituyen el objetivo principal de la terapia dirigida contra el cáncer.
Las pruebas genéticas tienen como objetivo identificar estas mutaciones, ya sean heredadas o adquiridas, para proporcionar un mapa preciso del tumor.
Objetivos principales de las pruebas genéticas para el cáncer
El objetivo de las pruebas genéticas va más allá del diagnóstico tradicional, ya que proporciona información crucial que influye en todo el plan de tratamiento. Los objetivos clave de las **pruebas genéticas del cáncer** incluyen:
1. Terapia dirigida:
- **Elección de la terapia dirigida:** Las pruebas identifican mutaciones genéticas que pueden ser tratadas con medicamentos específicos para detener el crecimiento de células cancerosas sin dañar las células sanas. Por ejemplo, la detección de una mutación del EGFR en el cáncer de pulmón orienta al médico a utilizar inhibidores del EGFR.
- **Determinación de la respuesta a la inmunoterapia:** Ciertas mutaciones o marcadores de inestabilidad genómica (como TMB y MSI) determinan si un paciente se beneficiará o no de la inmunoterapia.
2. Predicción del comportamiento del tumor (Pronóstico):
- **Predecir el curso futuro de la enfermedad:** El examen ayuda a predecir el comportamiento del tumor, si será agresivo y de rápida propagación o de crecimiento lento.
- **Predecir la respuesta del paciente a los medicamentos:** Esto ayuda a determinar la probabilidad de que un paciente responda a la quimioterapia o radioterapia, reduciendo así los tratamientos innecesarios y los efectos secundarios asociados.
3. Detección del riesgo de cáncer hereditario:
- **Cómo distinguir entre cáncer hereditario y no hereditario:** El examen ayuda a determinar si la infección es causada por una mutación genética que puede transmitirse a los miembros de la familia.
- **Gestión de riesgos:** Permite a los familiares en riesgo tomar medidas preventivas, como exámenes tempranos frecuentes o cirugía preventiva.
Pasos detallados para realizar una prueba de huella genética
El proceso de **huella genética** es complejo y preciso, y se lleva a cabo en laboratorios especializados. Si bien el método de recolección de muestras varía, el proceso de laboratorio sigue pasos estandarizados:
1. Recolección y calidad de la muestra: La muestra es la base de la precisión.
La muestra se suele recoger de dos formas principales:
- **Biopsia de Tejido:** Este es el método más común y preferido por su precisión primaria. Se toma una pequeña muestra directamente del tumor y se utiliza para el análisis genético directo de las células cancerosas.
- **Biopsia líquida:** Se utiliza en el análisis de ADN libre circulante (cfDNA) o ADN tumoral circulante (ctDNA).
2. Extracción de ADN:
Esta etapa es crucial para garantizar la calidad del análisis. El ADN se separa de las células o del plasma (en el caso de los análisis de sangre) mediante técnicas de laboratorio precisas y productos químicos para obtener una cantidad suficiente y pura de ADN.
3. Análisis genético y uso de técnicas avanzadas de NGS
La precisión de las pruebas genéticas depende de la tecnología utilizada para leer la secuencia genética. Aquí es donde entran en juego las tecnologías modernas:
Tecnología de secuenciación de próxima generación (NGS)
La tecnología NGS se considera el estándar de oro para el análisis genético integral. Esta tecnología avanzada permite:**
- **Detección integral:** Detecta cientos de genes a la vez en un solo análisis (Paneles de genes).
- **Velocidad y Precisión:** Lectura de secuencias de ADN a alta velocidad y a un menor costo que antes.
- **Descubrimiento de mutaciones raras**: Su capacidad para detectar mutaciones genéticas raras o nuevas que podrían no ser detectadas por tecnologías más antiguas.
Tecnología de reacción en cadena de la polimerasa (PCR)
Se utiliza para detectar mutaciones específicas previamente conocidas, como una o dos. Es rápido y adecuado para situaciones que requieren un resultado rápido o cuando el objetivo es buscar una mutación predicha.
4. Lectura de los resultados e interpretación del informe final
Una vez finalizado el proceso de secuenciación, la enorme cantidad de datos genéticos se analiza mediante programas informáticos especializados (bioinformática).
- **Comparación de bases de datos:** El genotipo del paciente se compara con conjuntos de datos globales masivos (como los conjuntos de datos COSMIC y ClinVar) para determinar el efecto de la mutación detectada en la función de la proteína y su relación con la enfermedad.
- **Interpretación del informe final:** Este paso lo realiza el oncólogo o genetista. Las mutaciones detectadas se relacionan con el **diagnóstico preciso**, el **plan de tratamiento específico** y el **pronóstico**.

La diferencia fundamental entre la prueba genética de la sangre (biopsia líquida) y la prueba de tejido
Distinguir entre análisis de sangre y análisis de tejido es un aspecto importante a la hora de realizar análisis genéticos de tumores. Cada uno tiene su función y sus ventajas.
Primero: Análisis de sangre (Biopsia líquida) – Análisis no invasivo
**La prueba de genes en sangre** se basa en el análisis del ADN de las células cancerosas circulantes (ctDNA), que es liberado por las células cancerosas que mueren o se descomponen.
- **Características principales:**
- **Fácil, rápido e indoloro:** No requiere ningún procedimiento quirúrgico ni anestesia, y es ideal para pacientes frágiles o que padecen otras enfermedades.
- **Monitoreo de la progresión de la enfermedad:** Esto es muy útil para monitorear la progresión de la enfermedad y la respuesta al tratamiento, ya que se puede realizar repetidamente para detectar la aparición de nuevas mutaciones de resistencia.
- **Evita biopsias difíciles:** Ideal para pacientes que son difíciles de biopsiar, especialmente en casos de tumores óseos o cerebrales.
- **Detección de heterogeneidad tumoral:** Esto muestra cambios en el tumor a lo largo del tiempo y en sus diversas ubicaciones de propagación.
- **Limitaciones (Defectos):**
- Es posible que no detecte todas las mutaciones, especialmente si la cantidad de ADN canceroso es muy pequeña, como en los cánceres tempranos.
- Menos preciso para determinar las características del tumor en etapas muy tempranas en comparación con el examen de tejido.
Segundo: Biopsia de tejido: el estándar de oro
El **examen de tejido** se basa en el examen de las células cancerosas directamente del tumor primario o de las metástasis.
- **Características principales:**
- **La prueba genética más precisa jamás realizada:** Proporciona la mayor cantidad de ADN tumoral, lo que garantiza la máxima precisión.
- **Revela las características completas del tumor:** Adecuado para el análisis integral del panel genético y la detección de marcadores complejos como mutaciones de fusión que son difíciles de detectar en la sangre.
- **Diagnóstico inicial:** Este es el método preferido para el diagnóstico inicial de la enfermedad.
- **Limitaciones (Defectos):**
- Requiere un procedimiento quirúrgico menor (biopsia), que puede causar dolor o complicaciones menores.
- A veces la muestra puede no ser suficiente para un análisis completo (Contenido tumoral insuficiente).
- No se puede repetir fácilmente para monitorear la respuesta al tratamiento.
¿Cuándo es recomendable realizar la huella genética?
Las pruebas genéticas se han convertido en una necesidad médica en muchos casos, y no se limitan a pacientes con cáncer avanzado. Se recomiendan en las siguientes situaciones:
1. Casos sospechosos de cáncer hereditario:
- **Una fuerte historia familiar de cáncer:** Especialmente si la enfermedad ha aparecido en varias generaciones o en muchos miembros de la familia.
- **La enfermedad aparece a temprana edad:** especialmente antes de los cincuenta años.
- **Cánceres raros o multitisulares**.
2. Planificación del tratamiento de cánceres comunes:
Las pruebas genéticas son esenciales antes de iniciar cualquier terapia dirigida, especialmente en cánceres que los estudios han demostrado que están directamente relacionados con mutaciones tratables:
- **Cáncer de pulmón:** Para detectar mutaciones en *EGFR*, *ALK*, *ROS1* y otros.
- **Cáncer colorrectal:** Para buscar mutaciones *KRAS*, *NRAS* y *BRAF*.
- **Cáncer de mama:** Para buscar mutaciones genéticas y adquiridas *HER2* y *BRCA*.
- **Cáncer de piel (melanoma):** Para buscar la mutación *BRAF*.
3. Casos de resistencia al tratamiento:
- **Cuando el paciente no responde al tratamiento convencional:** Si la quimioterapia o la radioterapia convencionales fallan, las pruebas genéticas pueden orientar el uso de una nueva línea de tratamiento dirigida.
- **En caso de recurrencia:** Para reevaluar las mutaciones, las células cancerosas pueden haber desarrollado una nueva mutación de resistencia.
Precisión y confiabilidad de las pruebas de huellas genéticas (¿Son precisos los resultados?)
La precisión de las pruebas genéticas para el cáncer se encuentra entre las más altas del diagnóstico médico moderno. Médicos de todo el mundo confían en ellas porque proporcionan datos cuantitativos y cualitativos sobre los cambios genéticos, en lugar de depender únicamente de las características fenotípicas de las células.
Tecnología y fiabilidad NGS garantizadas:
Al utilizar la tecnología NGS moderna, especialmente en muestras de tejido de alta calidad, la precisión en la detección de mutaciones alcanza niveles excelentes. Los análisis de sangre también han mejorado significativamente su precisión y ahora se utilizan con fiabilidad para la monitorización de enfermedades y la detección temprana de recaídas.
El impacto de la precisión en las decisiones de tratamiento:
Estudios a gran escala indican que las pruebas genéticas orientan las decisiones de tratamiento para los cánceres modernos, con valores entre 70% y 80%. Esto significa que la decisión de cambiar el tipo de tratamiento, añadir terapia dirigida o participar en un ensayo clínico depende directamente de los resultados de esta prueba.
En muchos casos, las pruebas genéticas son una causa directa de **mejores resultados del tratamiento y mayores tasas de recuperación**, porque garantizan que el paciente reciba un tratamiento específicamente diseñado para las mutaciones presentes en su tumor.
Puntos fuertes y papel futuro del análisis genético
El **Análisis Genético de Tumores** representa la fuerza impulsora de la Medicina de Precisión, y sus fortalezas se evidencian en lo siguiente:
1. Habilitación de la terapia dirigida:
- Ayuda a seleccionar un tratamiento preciso dirigido a la mutación genética específica, lo que aumenta la eficacia del tratamiento y reduce los efectos secundarios graves.
- Reduce tratamientos innecesarios que no beneficiarán al paciente, ahorrando tiempo, esfuerzo y recursos.
2. Seguimiento integral de la enfermedad:
- Ayuda a monitorear la enfermedad y determinar la probabilidad de recurrencia mucho después del tratamiento, especialmente cuando se utilizan análisis de sangre periódicos (biopsia líquida).
- Detecta cánceres hereditarios de forma temprana, permitiendo una intervención preventiva.
3. Ingresar a ensayos clínicos (Ensayos clínicos):
Muchos fármacos nuevos y prometedores en ensayos clínicos se basan en la focalización de mutaciones genéticas específicas. Los resultados de las pruebas genéticas son clave para que los pacientes sean aptos para estos ensayos, brindándoles acceso a tratamientos de vanguardia antes de que estén disponibles comercialmente.
4. Diagnóstico preciso:
Proporciona un diagnóstico más preciso del tipo de tumor y su clasificación biológica molecular, clasificación que ha adquirido mayor importancia que la clasificación histológica tradicional en muchos casos.
Desafíos del análisis genético y la interpretación clínica
A pesar del tremendo progreso, la aplicación de las pruebas genéticas enfrenta algunos desafíos que los científicos y los médicos están trabajando para superar:
1. Heterogeneidad tumoral:
No todas las células de un tumor son genéticamente idénticas. Una biopsia tomada de una sola zona puede no representar la imagen genética completa del tumor o sus metástasis. Esta es una de las razones por las que se desarrolló la biopsia líquida para abordar esta heterogeneidad.
2. Mutaciones de significado desconocido (VUS):
En ocasiones, el cribado detecta mutaciones cuyo papel clínico o patológico aún no se ha determinado por completo (variantes de significado incierto). Interpretar estas mutaciones requiere un esfuerzo considerable y el seguimiento de bases de datos globales actualizadas.
3. Costo y cobertura del seguro:
El costo de las pruebas genéticas integrales (NGS) puede ser alto y no todos los sistemas de seguro de salud las cubren completamente, aunque el costo de un tratamiento ineficaz a menudo excede el costo de las pruebas genéticas.
Resumen y perspectivas futuras de la huella genética
La **huella genética** es un paso esencial e indispensable en el diagnóstico y la planificación del tratamiento del cáncer en la década actual. Hemos pasado de un modelo único para todos a uno de **medicina personalizada de precisión**, donde las decisiones de tratamiento se basan en el perfil genético único de cada paciente.
Este examen avanzado no solo ayuda a comprender con precisión la naturaleza del tumor y a seleccionar el tratamiento más adecuado y eficaz, sino que también contribuye directamente a mejorar las probabilidades de recuperación y a reducir la carga de tratamientos innecesarios. A medida que las pruebas genéticas de nueva generación (NGS) continúan desarrollándose y surgen nuevas generaciones de terapias dirigidas, el papel fundamental del análisis genético tumoral seguirá creciendo, convirtiéndose en la mayor esperanza para pacientes y médicos en su lucha contra el cáncer.
Si usted o un miembro de su familia enfrenta un diagnóstico de cáncer, consultar a un oncólogo acerca de someterse a pruebas genéticas integrales es el primer paso y el más importante para garantizar que reciba las mejores y más precisas opciones de tratamiento disponibles a nivel mundial.